
LC-MS/MS的最新发展进一步降低了可达到的检测限。但在本文中,LC-MS/MS的最新进展特别用于获取更低的RSD,比之前采用此类多分析物方法所达到的RSD还要低得多。这种高度重现性能够在保证所有产品消费者健康与安全的同时解决标示量纠纷,最大程度减少过剩量,并维持利润。本应用纪要使用UPLC/MS/MS系统通过一种方法定量七种水溶性维生素,所有维生素的RSD值均小于3%。
对于使用婴儿配方奶粉和成人营养品的消费者来说,含人体健康必需维生素的强化配方被普遍认为是满足营养需求的必要条件。研究者们通过大量的研究从健康益处和安全角度确保能够提供相应含量的这些维生素1。
为确保产品在保质期内可以提供相应含量的维生素,制造商必须考虑到维生素会随时间发生分解,从而增加强化维生素的初始剂量进行弥补。由于这些维生素存在最高和最低含量限制,因此必需在富余与降解之间达到精确的平衡。精密和准确的维生素浓度测定就变得至关重要。在不同实验室中完成分析目标给本就相当复杂的维生素分析带来更大的挑战,研究者们几乎难以应对。要使实验室之间以及实验室内部的分析结果满足分析要求,具有良好的重现性,就必须减少实验中的变异因素。
LC-MS/MS技术日益广泛地应用于食品中强化维生素的定量分析2-5。 在选择性和灵敏度方面的优势,以及通过单次进样分析其中多种分析物的能力,使这一技术成为此类应用的最优之选。LC-MS/MS的最新发展进一步降低了可达到的检测限。但在本文中,LC-MS/MS的最新进展特别用于获取更低的RSD,比之前采用此类多分析物方法所达到的RSD还要低得多。这种高度重现性能够在保证所有产品消费者健康与安全的同时解决标示量纠纷,最大程度减少过剩量,并维持利润。
|
系统: |
ACQUITY UPLC |
|
色谱柱: |
ACQUITY HSS T3 C18, 1.8 μm, 1.0 X 100 mm |
|
柱温: |
60 °C |
|
进样体积: |
10 μL |
|
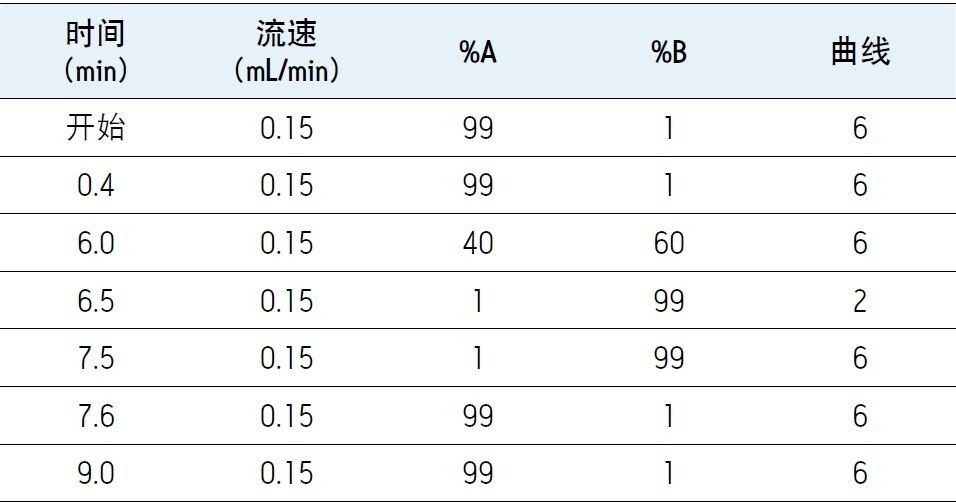
流速: |
0.15 mL/min |
|
流动相A: |
水 + 0.05% HCOOH以及0.01% HFBA |
|
流动相B: |
甲醇(含10 mM NH4OH) |
|
强清洗液: |
甲醇 |
|
弱清洗液: |
水 |
|
质谱仪: |
Xevo TQ-S |
|
电离模式: |
ESI+ |
|
毛细管电压: |
2.5 kV |
|
脱溶剂气温度: |
500 °C |
|
脱溶剂气流速: |
750 L/h |
|
源温度: |
150 ℃ |
|
锥孔气流速: |
300 L/h |
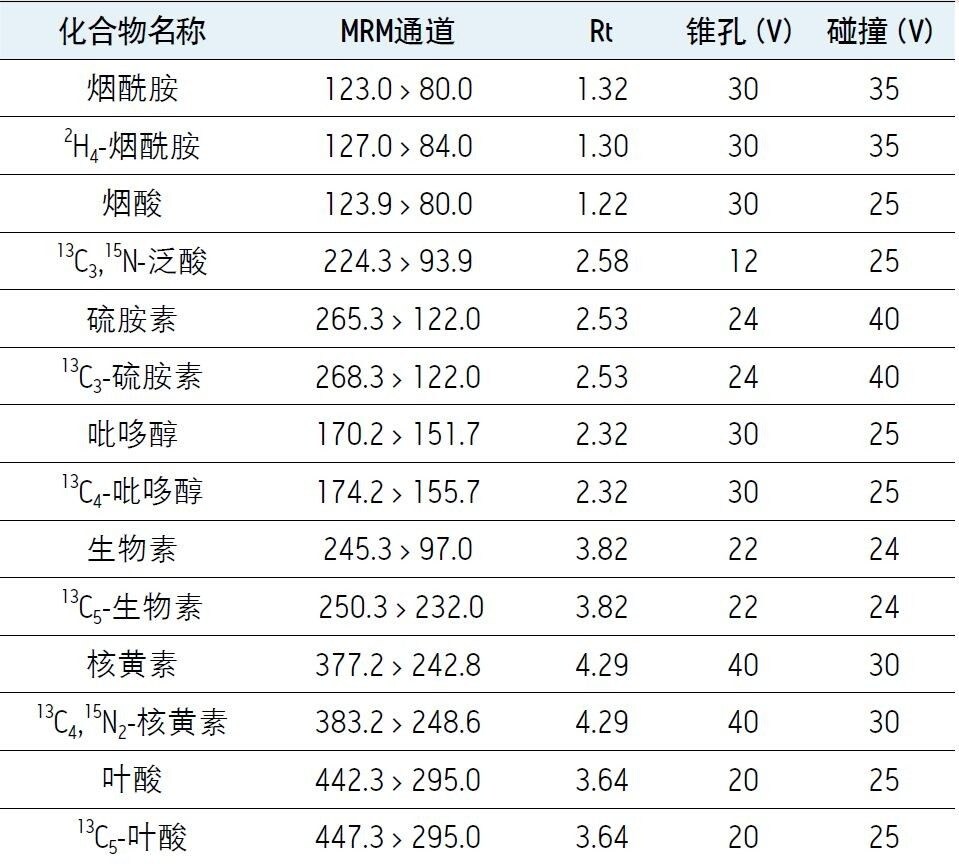
表2显示了各水溶性维生素所选的MRM通道、锥孔电压和碰撞能量及其内标物,以及预期的化合物保留时间。
在1%抗坏血酸溶液中制备七份含有全部分析维生素和同位素标记标准品的工作标准溶液,然后使用氢氧化铵调节pH值。
根据该方法的(专利)标准操作程序(SOP),精密称取一定量的样品。样品的量取决于要分析的具体产品。产品包括液态和粉末配方。加入每种维生素的同位素标记标准品。充分混匀样品后,在样品中加入25 mL的1%抗坏血酸。再次均匀混合,加入80 µL的30%氢氧化铵。再次混匀,静置10分钟。从稳定的样品中取将一份上清液,通过0.45 µm PTFE直接过滤到自动进样器小瓶中。
通过分析SOP制得的工作标准品和样品对于Xevo TQ-S分析而言浓度过高。为符合SOP要求,对调谐参数进行了优化,使响应值落在仪器的线性范围内。
图1展示了NIST SRM 1849a中各维生素的MRM色谱图示例。表3中给出了SRM 1849a中各维生素的计算含量,以及NIST报告的含量和预期范围。如表3所示,本方法的测得值与已发表值之间的一致性良好,且具有出色的精度(RSD)值。
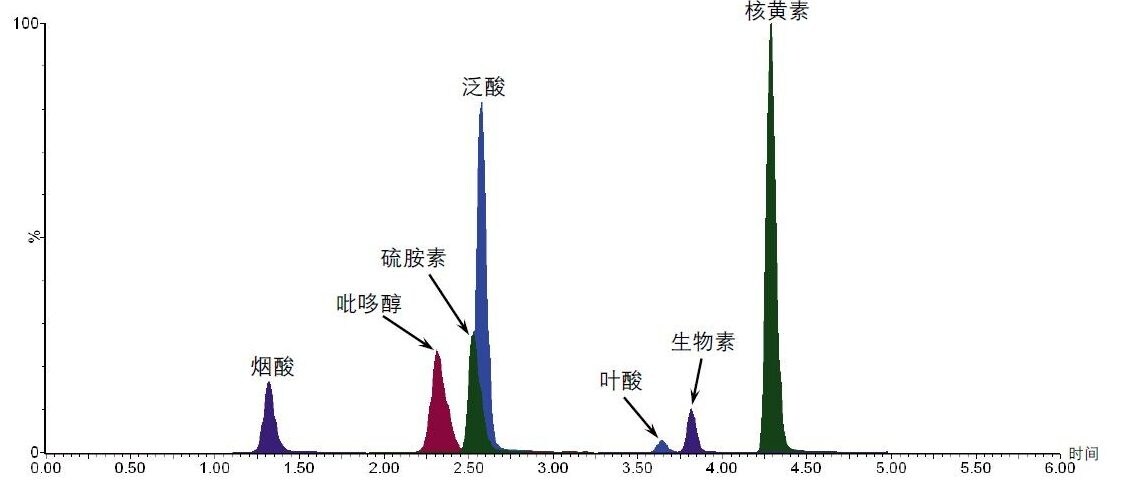
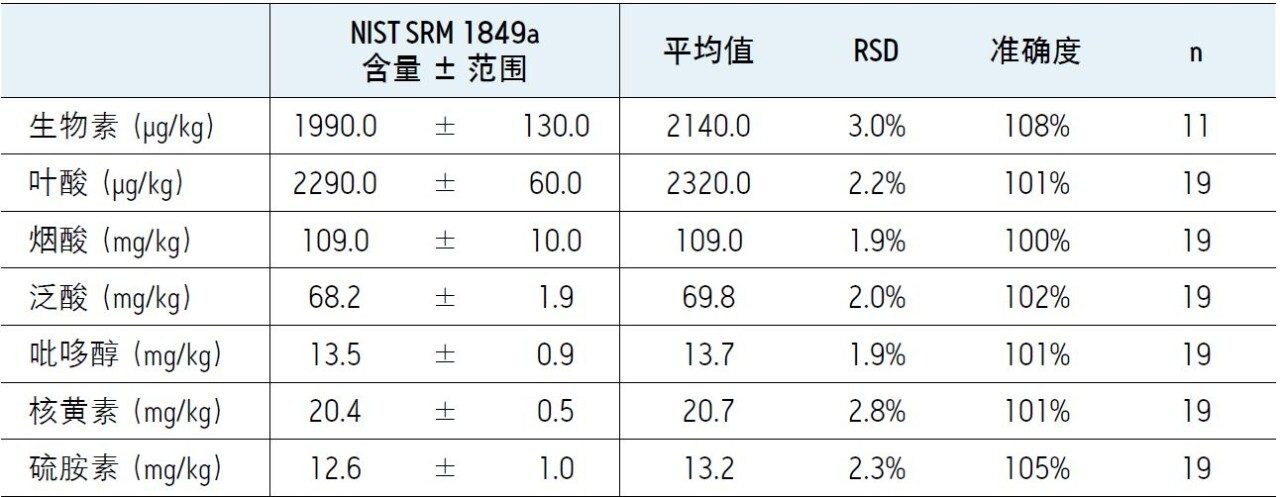
图2所示为各维生素最低含量标准品的MRM色谱图示例,以及它们的校准曲线。七条校准曲线均显示r2值<0.999。表4中给出了四个单独日的一日内变化,范围介于0%到2.8%之间。表5中给出了各维生素的最低工作标准溶液浓度。
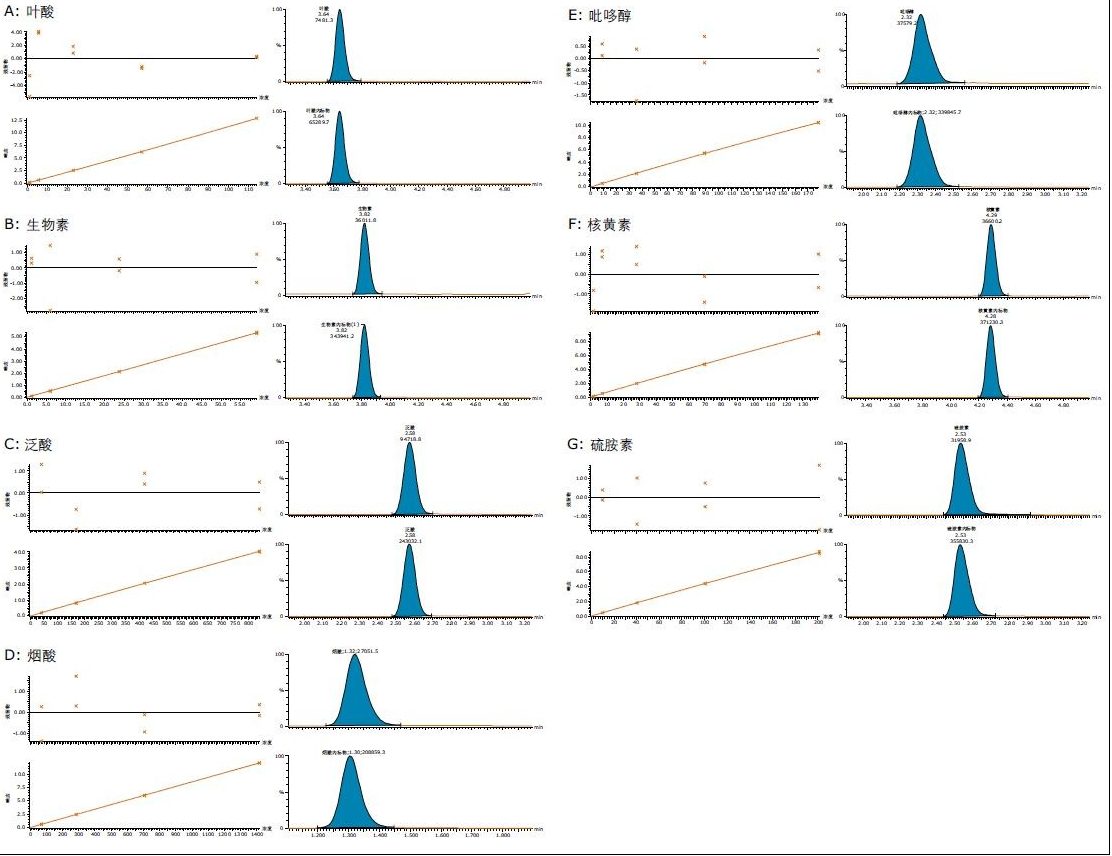
图2.校准曲线与残余物图,以及最低含量标准品和各维生素内标物的MRM色谱图。最低含量标准品的浓度如下所列。
A:叶酸,1.14 ng/mL
B:生物素,1.18 ng/mL
C:泛酸,8.40 ng/mL
D:烟酸,14.17 ng/mL
E:吡哆醇,1.78 ng/mL
F:核黄素,1.40 ng/mL
G:硫胺素,2.10 ng/mL
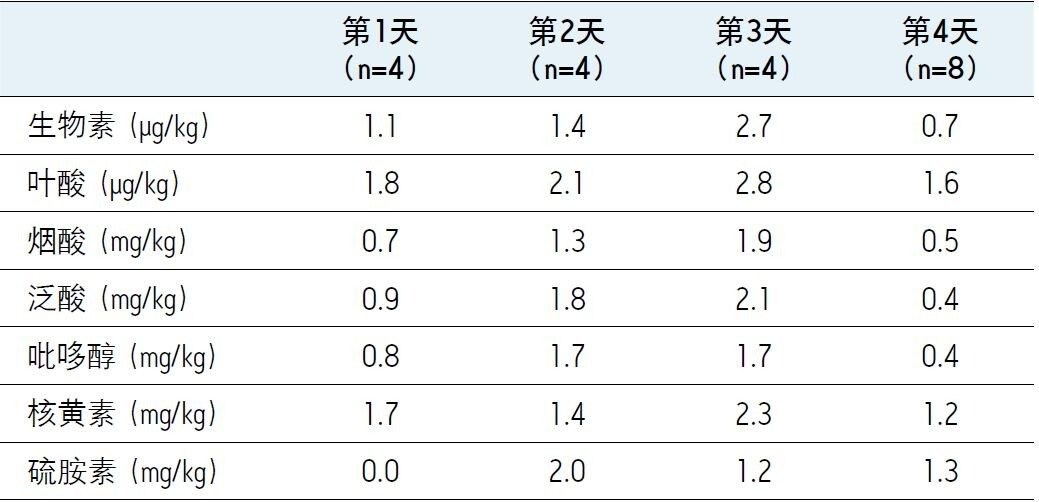
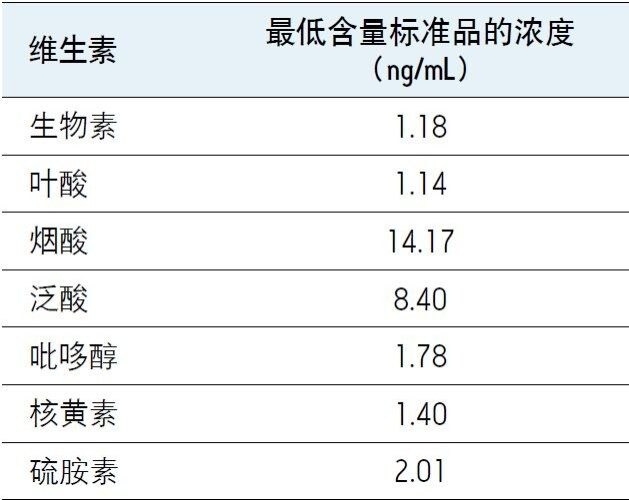
文献报告有强化配方产品中维生素分析的日内和日间变异。Goldschmidt和Wolf2发表了一种使用MS检测的HPLC分析方法,对于烟酰胺、吡哆醇和泛酸,此方法测得的RSD小于3%。对于核黄素和生物素,测得的RSD约为5%,但是对于硫胺素和叶酸,报告所得RSD通常大于5%。Huang等人3研究发现,市售婴儿配方奶粉的八次重复实验重现性低于5%。据Zhang等人4报告,14种维生素和类维生素化合物的日内变异范围为1.17%至7.81%。日间变异报告范围介于2.61%至8.42%之间。如表4所示,对于所分析的各种化合物,与文献方法相比,本方法的日内变异获得显著改善。为评估本方法的重现性,我们在8个月时间段内的19个不同日期中进行了19次独立制备。在这段时间里,曾更换生物素的内标物,因此表3中只包括了使用最终生物素内标物所得的测定结果(即最后11次分析的结果)。使用旧生物素内标物所得测定结果的RSD为2.0%,与NIST值相比的准确度为102%(n=8)。因此,两种生物素内标物均适用于本方法。总体而言,本研究的变异性通常低于2.5%,如表3所示。只有生物素和核黄素的变异性略高于此值。所有分析物的准确性介于100%至108%之间。
720004690ZH,2013年5月