在本应用纪要中,我们将SYNAPT XS与沃特世UNIFI代谢物鉴定应用解决方案联用,鉴定小鼠血浆中吉非替尼(易瑞沙)的药物相关代谢物。
利用具有离子淌度功能的质谱分析法对药物代谢物进行高灵敏度、快速并且准确的鉴定
药物代谢研究是药物发现与开发过程的重要组成部分,可在早期淘汰具有不利特性的分子,筛选出更具潜力的化合物。代谢物分析和鉴定在该过程中起关键作用,可确保安全性评估模型能够提供足够的全身暴露量以便对人体进行给药研究。质谱分析(MS),尤其是高分辨质谱(HRMS),现已成为药物代谢物分析和鉴定的首选平台1。 但是,高通量代谢物鉴定中仍存在多项挑战,包括代谢物共流出和内源性干扰、代谢位点的确定以及官能团化或偶联的确认。
具有离子淌度(IM)功能的MS分析兼具HRMS的强大功能和气相离子淌度技术的分离能力,可分离共流出代谢物或其它化合物(内源或外源),从而得到更清晰的谱图并提高子离子分子来源鉴定结果的可信度。近来,准确测定和预测气相碰撞截面(CCS)值的功能也使正确的结构鉴定和代谢区域化结果变得更加可靠。
SYNAPT XS高分辨率质谱仪是沃特世HRMS产品组合中具有离子淌度功能的最新款QTof质谱仪。SYNAPT XS高分辨率系统配备StepWave XS,可用于提高分析灵敏度并增强离子传输,还配备延长飞行管用于提高分辨率。本文将SYNAPT XS与沃特世UNIFI代谢物鉴定应用解决方案联用,鉴定小鼠血浆中吉非替尼(易瑞沙)的药物相关代谢物。
吉非替尼是一种具有活性和选择性的表皮生长因子受体(EGFR;HER1)酪氨酸激酶抑制剂,口服用于治疗非小细胞肺癌,商品名为易瑞沙2-4。 之前的研究表明吉非替尼经过广泛的首过代谢后会形成各种代谢物2,3。 这些研究所用方法的色谱分析时间为15~45 min,才能达到可靠鉴定药物代谢物所需要的MS和MS-MS谱图质量。该通量达不到现代药物发现的要求。为解决通量问题,我们采用了基于梯度洗脱的反相UPLC-IMS/MS,总分析时间5 min。代谢物鉴定完成后,将离子淌度系统生成的CCS值与预测算法配合使用,确认鉴定结果和代谢区域。
对小鼠进行吉非替尼静脉注射(IV)和口服(PO)给药,剂量分别为10 mg/Kg和50 mg/Kg。通过尾部采血获取24小时内的血样。选择混合2~6小时时间点的样品进行分析。用三倍样品体积的甲醇(含0.1%甲酸)进行蛋白沉淀,制得小鼠血浆样品。将样品-甲醇溶液涡旋混合,然后在25000 g离心力下离心5 min。取所得上清液10 µL,用490 µL 50:50的甲醇/水将其稀释至500 µL。
|
LC条件: |
|
|---|---|
|
LC系统: |
ACQUITY UPLCI-Class |
|
色谱柱: |
2.1 x 100 mm BEH C18 1.7 mm |
|
柱温: |
60℃ |
|
样品温度: |
4 °C |
|
进样体积: |
2 mL |
|
流速: |
650 mL/min |
|
流动相A: |
0.1%甲酸水溶液+ 10 mM醋酸铵 |
|
流动相B: |
0.1%甲酸的乙腈溶液 |
|
梯度: |
流动相B在2.9 min内以线性梯度从5%增加至50%。然后用95%流动相B冲洗1.5 min。 |
|
MS系统: |
SYNAPT XS高分辨率质谱仪 |
|
分析仪模式: |
分辨率 |
|
电离模式: |
ESI+ |
|
全扫描MS: |
50-1200 m/z |
|
扫描时间: |
0.3 s |
|
采集模式: |
HDMSE |
|
毛细管电压: |
3.0 kV |
|
碰撞能量(LE): |
4 eV |
|
碰撞能量范围(HE): |
20-40 eV |
|
IM缓冲气体: |
氮 |
|
IM波高: |
40 V |
|
IM波速: |
650 m/s |
|
MS软件: |
MassLynx 4.2版 |
|
信息学软件: |
UNIFI 1.9.4科学信息系统 |
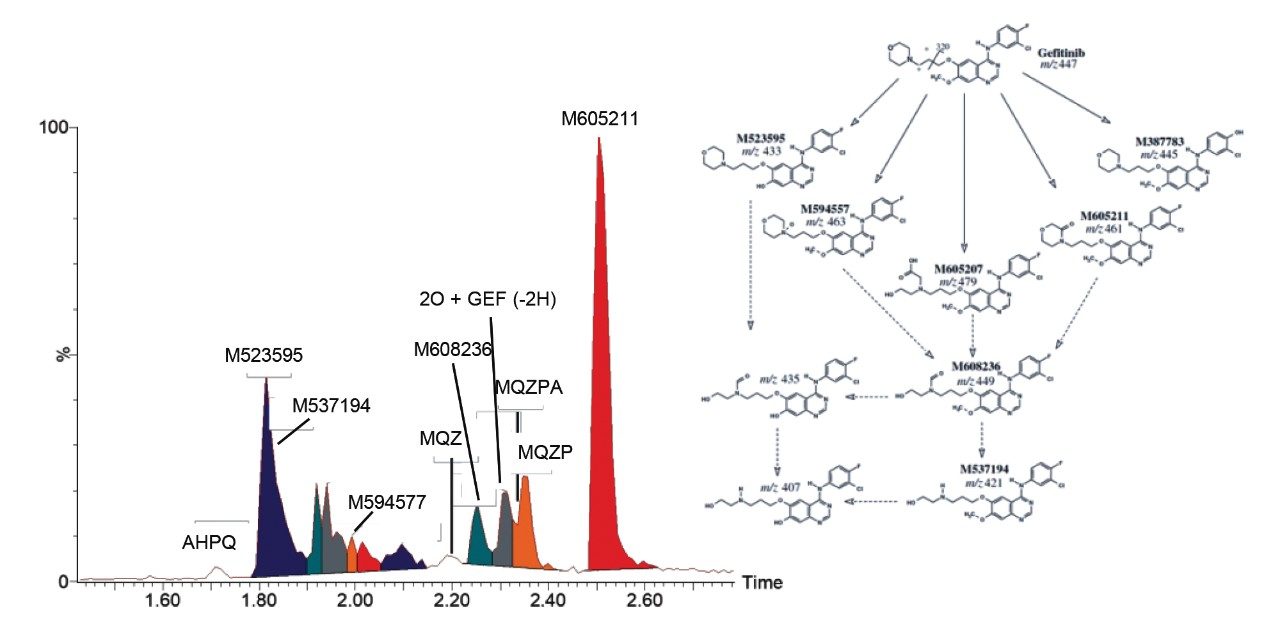
如前所述,本文利用基于SYNAPT XS高分辨率质谱仪的5 min LC-HDMSE方法对吉非替尼给药组小鼠血浆样品中的药物相关代谢物进行检测和进一步表征。将所得数据传输至UNIFI科学信息系统通过代谢物鉴定工作流程进行数据分析。吉非替尼流出峰的保留时间为1.88 min,并且在1.72~2.51 min范围内的流出峰中鉴定共出10种药物相关代谢物(图1)。尽管分析时间短,但方法总体上的专属性和选择性足以检出和分离多数代谢物。
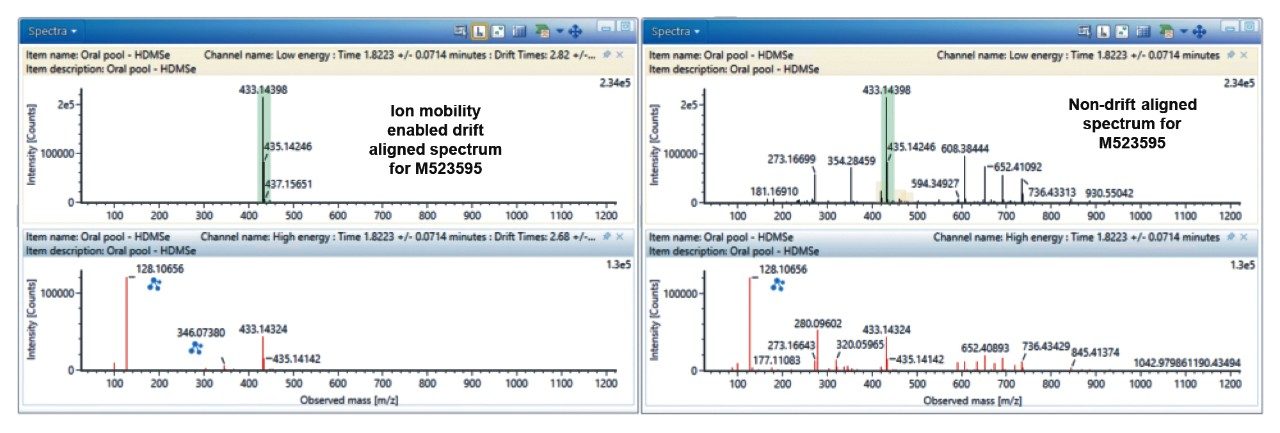
在进行代谢物鉴定时,尤其是使用自动化软件驱动分析时,所面临的一项主要难题是需要得到“清晰”的MS谱图进行解析。离子淌度技术为LC-MS分析提供了额外的正交分离维度,该技术依据分子离子的大小、形状和电荷进行分析。离子淌度分离结果通过离子漂移时间(ms)记录,可用于在数据视图中创建筛选条件以排除那些在色谱分析时虽然共流出但漂移时间不同的离子。谱图质量提升示例见图2,O-去甲基代谢物(M523595)分析。在本例中,采用离子淌度技术得到的经漂移时间校准的母离子和子离子MS谱图明显比未经漂移时间校准的数据谱图清晰,这是因为在未采用IMS技术的MS和MS-MS数据中存在大量与药物不相关的内源性峰。与药物代谢物相关的346.0738 m/z峰在未采用IMS技术得到的数据中不可见,但在经IMS漂移时间校准的数据中可以轻松找到。谱图质量的这一提升简化了手动型和软件赋能型代谢物鉴定,并因此提高了鉴定速度。
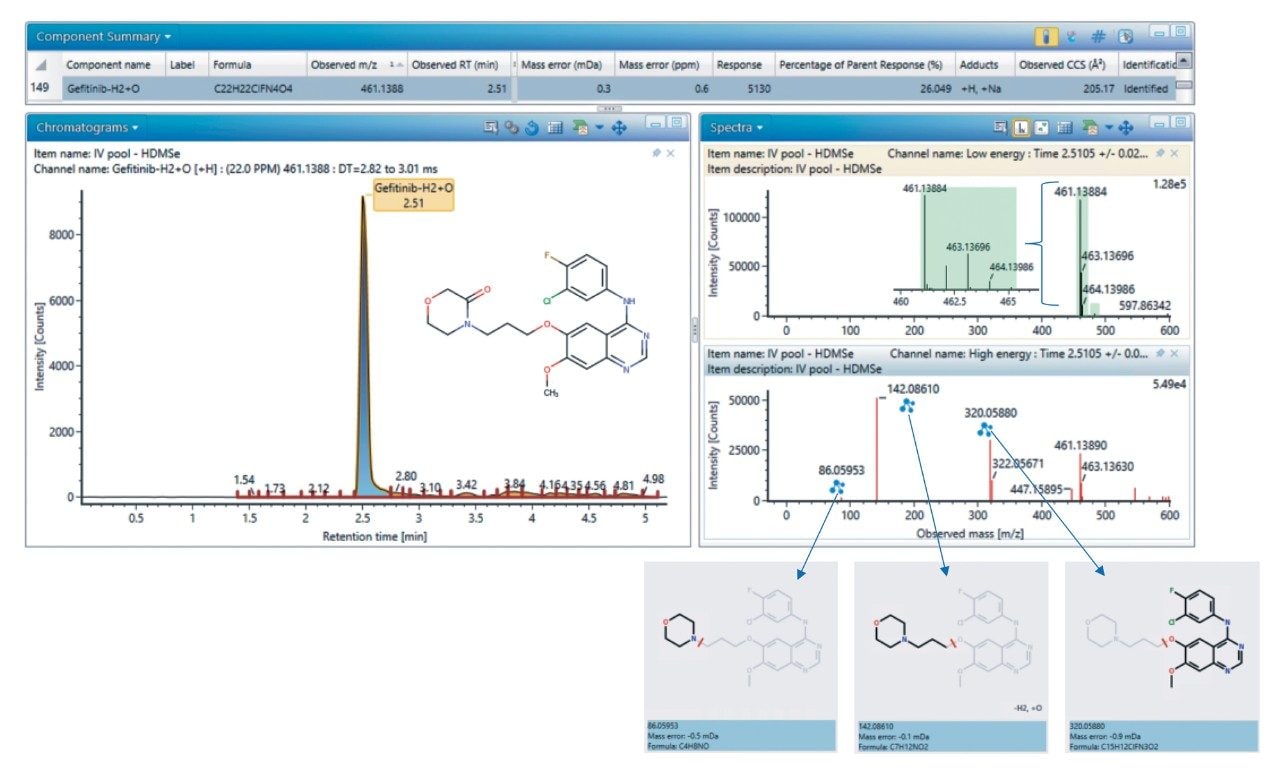
吉非替尼的分子式为C22H24ClFN4O3,其单同位素分子量为446.1521 Da。母离子表现出特征性氯同位素分布模型,基峰m/z值为447.1598(质量数误差0.2 ppm)。在m/z = 320.0597和128.1078处观察到两种主要子离子。该信息连同官能团化和偶联常见代谢途径相关知识将用于吉非替尼代谢物的检测和鉴定。将得到的LC-MS数据传输至UNIFI科学信息系统通过代谢物鉴定工作流程进行分析。如需更加完整的软件介绍,请参阅https://www.waters.com/webassets/cms/library/docs/720006106en.pdf。简言之,即根据代谢物母离子和子离子的m/z以及单Cl同位素分布模型鉴定代谢物。吉非替尼通过细胞色素p450 3A4代谢,主要代谢途径为吗啉环氧化以及喹唑啉核上甲氧基取代基的O-去甲基化2。 经鉴定,O-去甲基代谢物(M523595)为主要代谢物,在1.76 min处流出,羰基代谢物(M605211)的丰度次之。测得M605211母离子的m/z为461.1388(质量数误差<1 ppm),表现为典型的单Cl同位素分布模型。检出的三种主要子离子:320.0588 m/z(C15H12ClFN3O2,误差0.9 mDa)、142.861 m/z(C7H12NO2,误差0.1 mDa)和86.0595 m/z(C4H8NO,误差0.5 mDA)。图3展示的是利用UNIFI软件对M605211进行结构解析。SYNAPT XS系统能够提供高质量精度的优质MS和MS/MS谱图,从而实现可靠的代谢物鉴定。
具有离子淌度功能的MS不仅能够提供额外的分离维度,还能够准确测定碰撞截面(CCS)。CCS能够为鉴定提供额外的切入点(例如保留时间和准确质量数),从而实现化合物表征。CCS计算和预测方面的最新进展已能够准确、快速预测CCS值,以便为结构鉴定提供支持信息5,6。为评价CCS预测在本研究中的应用效果,先使用之前报道的机器学习方法计算了吉非替尼代谢物的CCS值,然后将其与测定值进行比较6。 所得数据如图5和表1所示。从上述结果可以看出,吉非替尼代谢物CCS值的预测结果与测定结果之间存在显著的相关性,其平均绝对误差(MAE)为1.8%。因此CCS预测是有效研究方向,可为IM实验的结构表征提供支持信息。
SYNAPT XS系统是一款高分辨率、高灵敏度并且具有离子淌度功能的质谱仪,配合UNIFI科学信息系统和代谢物鉴定工作流程使用时,可作为快速鉴定代谢物的理想选择,能够用于支持药物发现。离子淌度MS可利用IMS池的正交分离功能分离邻近洗脱的代谢物以及内源性成分或异构体,从而提供更加清晰的MS和MS/MS谱图,有助于提高代谢物鉴定结果的可信度。此外,具有离子淌度功能的HRMS还能够测定分子特定的碰撞截面数据,而该数据可配合机器学习预测软件共同用于确定代谢物的结构归属。
720006908ZH,2020年6月