
本应用简报证明,应用漂移时间以及保留时间进行谱图校准能够明显改善谱图清晰度,有助于对右美沙芬温育代谢物/降解物进行结构表征分析。
离子淌度分离技术与MSE采集(HDMSE)联用可在药物发现或开发中显著提升非数据依赖型采集(DIA)模式下代谢物鉴定的可信度。
灵敏并且准确的药物代谢物和/或药物降解产物归属是DMPK研究的关键。提高鉴定结果的可信度有助于在化合物发展为候选药物之前对其有效性和安全性进行快速、准确的评估。代谢物的基质环境非常复杂,因此进行准确鉴定非常困难。基质中可能包括会与目标分析物共流出的化合物或是质量数与目标分析物相近的化合物。上述情况均会产生干扰,进而影响峰面积估算或降低鉴定结果的可信度1。
将离子淌度分离技术与MSE联用进行HDMSE采集可根据气相漂移时间(测定单位:ms)分离共流出成分2。借助沃特世UNIFI科学信息系统(或其它CCS处理软件)的数据处理引入基于漂移时间的母离子分离可大幅改善谱图清晰度,并且能够为化合物附加与标准品或理论值作用相当的唯一标识。因此,可根据以下各项鉴定化合物:LC保留时间、准确质量数、碰撞截面(CCS)值以及更具体、更具选择性的母离子和碎片离子谱图。
从结构解析的角度来看,仅显示各母离子独有的碎片离子,能够进一步提升化合物鉴定、归属和定量结果的可信度。因此,分析人员能够获得数据依赖型采集(DDA)才能达到的谱图清晰度,且无需生成排除或包含表(有可能会排除关键离子)。
离子淌度分离(IMS)能够根据分析物的形态结构分离共流出分析物,原理是形态结构会改变其通过充满气体的离子淌度池的速度。增加此分离手段后,LC保留时间相同的分析物乃至同种化合物的异构体均可实现分离。在碰撞诱导解离(CID)碎裂(HDMSE)前应用该技术,可利用唯一漂移时间(通过离子淌度池)生成每种分析物各自的碎片离子谱图,因此所得到的碎片离子谱图清晰,不受共流出基质化合物干扰。
在分析候选药物的潜在代谢物或降解产物时,上述化合物的丰度可能会非常低。因此,基质中的共流出干扰有可能掩盖目标分析物或增加可靠归属的复杂程度。图1a是未采用IMS时右美沙芬代谢物2x + O的谱图。高能量(碎片离子)谱图(下图)表明存在大量共流出基质化合物干扰,干扰物离子信号强于目标分析物的真实子离子,占据主导地位。图1b是采用IMS功能分析相同代谢物时得到的谱图。在使用漂移时间作为目标分析物唯一标识的条件下,高能量谱图中干扰碎片的数量(上图)大幅减少。更加清晰的高能量谱图能够加快解析速度并提高分析物鉴定和结构归属的可信度。
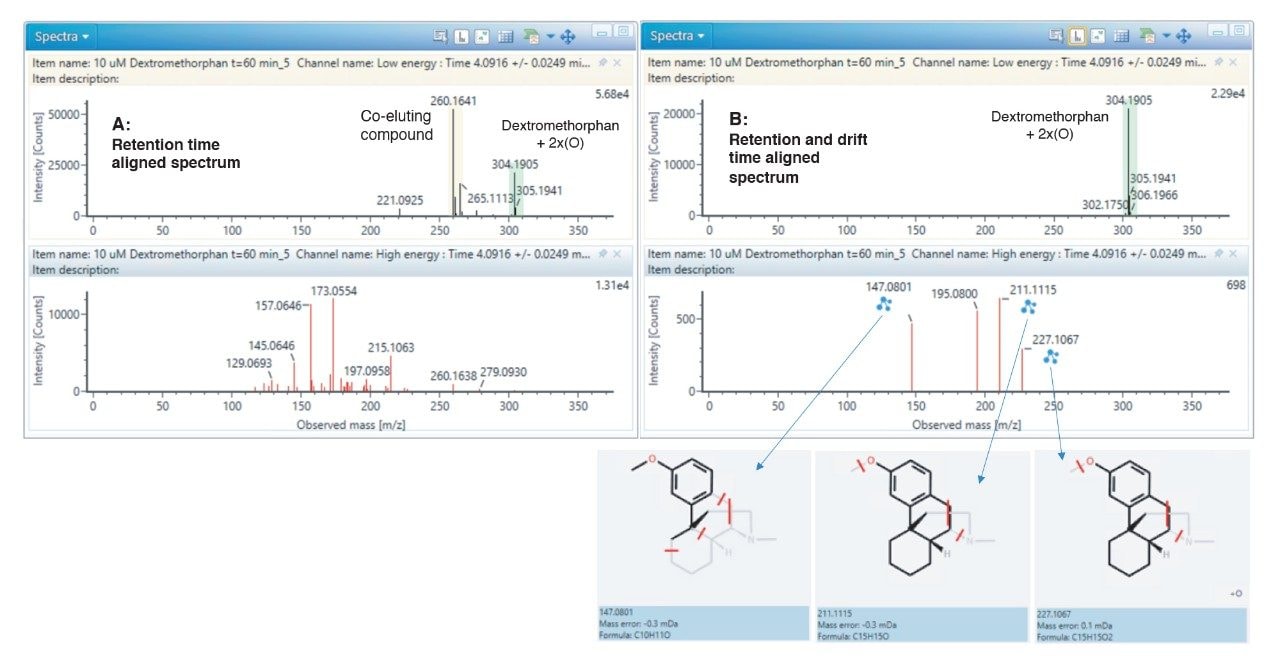
本研究数据展示了离子淌度分离技术与DIA联用在DMPK研究中所具有的优势。该正交分离技术的使用能够大幅提升药物代谢和降解产物鉴定的可信度和速度。右美沙芬代谢物2x + O子离子的信号相对弱于干扰基质离子,无法通过传统的LC-MS分析技术分离,进而增加归属的复杂程度。引入离子淌度维度后再分析相同的数据,基质子离子被移除,从而实现对代谢物子离子的轻松鉴定和可靠归属。
720006919ZH,2020年6月